Método pode penetrar mais profundamente em tecidos vivos.

Adam Zewe | MIT News
A imagem metabólica é um método não invasivo que permite a médicos e cientistas estudar células vivas utilizando luz laser, ajudando-os a avaliar a progressão de doenças e as respostas aos tratamentos.
No entanto, a luz se dispersa ao penetrar em tecidos biológicos, limitando sua profundidade de penetração e prejudicando a resolução das imagens capturadas.
Agora, pesquisadores do MIT desenvolveram uma nova técnica que mais do que dobra o limite usual de profundidade da imagem metabólica. Esse método também aumenta a velocidade de captura, resultando em imagens mais ricas e detalhadas.
Essa nova técnica não exige o pré-processamento do tecido, como cortes ou coloração com corantes. Em vez disso, um laser especializado ilumina profundamente o tecido, fazendo com que certas moléculas intrínsecas dentro das células e dos tecidos emitam luz. Isso elimina a necessidade de alterar o tecido, oferecendo uma representação mais natural e precisa de sua estrutura e função.
Os pesquisadores alcançaram isso personalizando de forma adaptativa a luz laser para tecidos profundos. Utilizando um modelador de fibras recentemente desenvolvido — um dispositivo controlado por meio de sua curvatura —, eles podem ajustar a cor e os pulsos de luz para minimizar a dispersão e maximizar o sinal à medida que a luz penetra mais profundamente no tecido. Isso permite que eles enxerguem muito mais longe em tecidos vivos e capturem imagens mais nítidas.
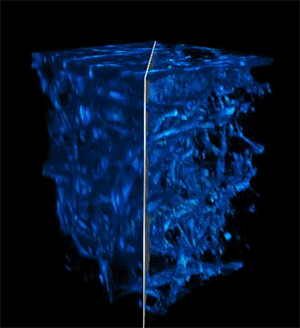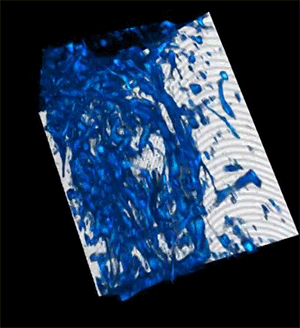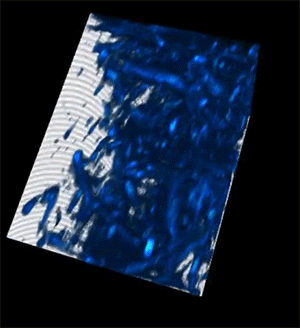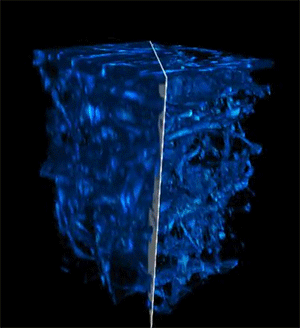
A maior profundidade de penetração, velocidades mais rápidas e resolução mais alta tornam esse método particularmente adequado para aplicações de imagem desafiadoras, como pesquisas sobre câncer, engenharia de tecidos, descoberta de medicamentos e estudo de respostas imunológicas.
“Este trabalho demonstra uma melhoria significativa em termos de penetração de profundidade para imagens metabólicas sem marcação. Ele abre novas possibilidades para o estudo e exploração de dinâmicas metabólicas em profundidade em biossistemas vivos”, diz Sixian You, professora assistente no Departamento de Engenharia Elétrica e Ciência da Computação (EECS), membro do Laboratório de Pesquisa em Eletrônica e autora principal de um artigo sobre essa técnica de imagem.
O artigo também conta com a coautoria de Kunzan Liu, estudante de pós-graduação em EECS; Tong Qiu, pós-doutoranda no MIT; Honghao Cao, estudante de pós-graduação em EECS; Fan Wang, professora de Ciências do Cérebro e Cognitivas; Roger Kamm, professor distinto Cecil e Ida Green de Engenharia Biológica e Mecânica; Linda Griffith, professora de Inovação no Ensino de Engenharia no Departamento de Engenharia Biológica; além de outros colegas do MIT. A pesquisa foi publicada na Science Advances.
Foco em laser
Este novo método se encaixa na categoria de imagens sem marcação, o que significa que o tecido não é manchado previamente. A coloração cria contraste, o que ajuda o biólogo clínico a visualizar melhor os núcleos celulares e proteínas. No entanto, a coloração normalmente exige que o biólogo faça cortes e seções na amostra, um processo que frequentemente mata o tecido e torna impossível estudar processos dinâmicos em células vivas.
Nas técnicas de imagem sem marcação, os pesquisadores usam lasers para iluminar moléculas específicas dentro das células, fazendo com que emitam luz de diferentes cores, revelando vários conteúdos moleculares e estruturas celulares. No entanto, gerar a luz laser ideal com certos comprimentos de onda e pulsos de alta qualidade para imagens de tecidos profundos tem sido desafiador.
Os pesquisadores desenvolveram uma nova abordagem para superar essa limitação. Eles usam uma fibra multimodo, um tipo de fibra óptica capaz de carregar uma quantidade significativa de energia, e a acoplam a um dispositivo compacto chamado “modelador de fibra”. Esse modelador permite que eles modifiquem com precisão a propagação da luz, alterando adaptativamente a forma da fibra. Curvar a fibra muda a cor e a intensidade do laser.
Baseando-se em trabalhos anteriores, os pesquisadores adaptaram a primeira versão do modelador de fibra para uma imagem metabólica multimodal mais profunda.
“Nós queremos canalizar toda essa energia nas cores que precisamos, com as propriedades de pulso que requeremos. Isso nos dá maior eficiência de geração e uma imagem mais nítida, mesmo em tecidos profundos”, diz Cao.
Depois de construir o mecanismo controlável, os pesquisadores desenvolveram uma plataforma de imagem para aproveitar a potente fonte de laser e gerar comprimentos de onda mais longos de luz, essenciais para uma maior penetração nos tecidos biológicos.
“Acreditamos que esta tecnologia tem o potencial de avançar significativamente a pesquisa biológica. Ao torná-la acessível e acessível para laboratórios de biologia, esperamos capacitar os cientistas com uma ferramenta poderosa para a descoberta”, diz Liu.
Aplicações dinâmicas
Quando os pesquisadores testaram seu dispositivo de imagem, a luz foi capaz de penetrar mais de 700 micrômetros em uma amostra biológica, enquanto as melhores técnicas anteriores conseguiam atingir apenas cerca de 200 micrômetros.
“Com esse novo tipo de imagem profunda, queremos olhar para amostras biológicas e ver algo que nunca vimos antes”, acrescenta Liu.
A técnica de imagem profunda permitiu que eles vissem células em vários níveis dentro de um sistema vivo, o que pode ajudar os pesquisadores a estudar mudanças metabólicas que acontecem em diferentes profundidades. Além disso, a maior velocidade de imagem permite reunir informações mais detalhadas sobre como o metabolismo de uma célula afeta a velocidade e a direção de seus movimentos.
Esse novo método de imagem poderia impulsionar o estudo de organoides, que são células engenheiradas que crescem para imitar a estrutura e função dos órgãos. Pesquisadores nos laboratórios de Kamm e Griffith são pioneiros no desenvolvimento de organoides cerebrais e endometriais que crescem como órgãos para avaliação de doenças e tratamentos.
No entanto, tem sido desafiador observar com precisão os desenvolvimentos internos sem cortar ou manchar o tecido, o que mata a amostra.
Essa nova técnica de imagem permite que os pesquisadores monitorem de forma não invasiva os estados metabólicos dentro de um organoide vivo enquanto ele continua a crescer.
Com essas e outras aplicações biomédicas em mente, os pesquisadores planejam buscar imagens de ainda maior resolução. Ao mesmo tempo, estão trabalhando para criar fontes de laser de baixo ruído, o que poderia permitir imagens mais profundas com menor dosagem de luz.
Eles também estão desenvolvendo algoritmos que reagem às imagens para reconstruir as estruturas 3D completas das amostras biológicas em alta resolução.
A longo prazo, esperam aplicar essa técnica no mundo real para ajudar os biólogos a monitorar a resposta a medicamentos em tempo real, ajudando no desenvolvimento de novos medicamentos.
“Ao permitir imagens metabólicas multimodais que penetram mais profundamente nos tecidos, estamos proporcionando aos cientistas uma capacidade sem precedentes de observar sistemas biológicos não transparentes em seu estado natural. Estamos empolgados em colaborar com clínicos, biólogos e bioengenheiros para expandir os limites dessa tecnologia e transformar essas descobertas em avanços médicos no mundo real”, diz You.
“Este trabalho é empolgante porque usa métodos inovadores de feedback para imagem do metabolismo celular em tecidos mais profundos em comparação com as técnicas atuais. Essas tecnologias também oferecem altas velocidades de imagem, que foram usadas para descobrir dinâmicas metabólicas únicas da motilidade de células imunes dentro dos vasos sanguíneos. Eu espero que essas ferramentas de imagem sejam fundamentais para descobrir conexões entre função celular e metabolismo dentro de sistemas vivos dinâmicos”, diz Melissa Skala, pesquisadora no Morgridge Institute for Research, que não participou deste trabalho.
“A capacidade de adquirir imagens multifotônicas de alta resolução com base no contraste de autofluorescência de NAD(P)H de forma mais rápida e profunda nos tecidos abre as portas para o estudo de uma ampla gama de problemas importantes”, acrescenta Irene Georgakoudi, professora de engenharia biomédica da Universidade Tufts, que também não participou desse trabalho. “A obtenção de imagens de tecidos vivos o mais rápido possível sempre que se avalia a função metabólica é sempre uma grande vantagem em termos de garantia da relevância fisiológica dos dados, amostragem de um volume significativo de tecido ou monitoramento de mudanças rápidas. Para aplicações em diagnóstico de câncer ou em neurociência, a geração de imagens mais profundas – e mais rápidas – nos permite considerar um conjunto mais rico de problemas e interações que não foram estudados em tecidos vivos antes.”
Essa pesquisa é financiada, em parte, por fundos de inicialização do MIT, um prêmio CAREER da Fundação Nacional de Ciências dos EUA, uma bolsa presidencial do MIT Irwin Jacobs e Joan Klein e uma bolsa Kailath do MIT.
Reproduzido com permissão do MIT News.






