Ferramenta de Precisão para Manipulação do DNA Mitocondrial
Muitas doenças mitocondriais têm sido difíceis de estudar e tratar devido aos desafios inerentes ao acesso ao DNA mitocondrial (mtDNA). Agora, pesquisadores do Japão otimizaram compostos direcionados às mitocôndrias que podem modificar seletivamente a proporção entre mtDNA normal e mutante em células-tronco derivadas de pacientes. Essa tecnologia permite a criação de modelos de pesquisa com diferentes cargas de mutações e demonstra potencial como estratégia terapêutica para reduzir o mtDNA mutante em pacientes, oferecendo esperança para o tratamento de doenças mitocondriais.
As doenças mitocondriais afetam aproximadamente 1 em cada 5.000 pessoas no mundo, causando sintomas debilitantes que vão desde fraqueza muscular até episódios semelhantes a derrames. Algumas dessas condições resultam de mutações no DNA mitocondrial, o material genético presente nessas organelas. Para pacientes com a mutação comum m.3243A>G — que pode causar a síndrome MELAS (miopatia mitocondrial, encefalopatia, acidose lática e episódios semelhantes a AVC), além de diabetes mellitus — os tratamentos ainda são limitados.
Um dos principais desafios na pesquisa de doenças mitocondriais é que os pacientes geralmente possuem uma mistura de mtDNA normal e mutante em suas células. Essa condição, chamada de heteroplasmia, dificulta o desenvolvimento de terapias direcionadas, já que a proporção entre mtDNA normal e mutante pode variar significativamente de um tecido para outro.
Além disso, a pesquisa básica atual sobre mutações no mtDNA enfrenta obstáculos importantes devido à falta de modelos de doenças. A relação complexa entre a carga mutacional (percentual de mtDNA mutante) e a gravidade da doença ainda é pouco compreendida, em parte porque não existem ferramentas para manipular precisamente os níveis de heteroplasmia em ambas as direções. Sem a capacidade de criar modelos celulares com diferentes cargas de mutações, os cientistas não conseguem estudar de forma eficaz como diferentes percentuais de mtDNA mutante se relacionam com a manifestação da doença.
Diante desse cenário, uma equipe de pesquisa liderada pelo professor assistente sênior Naoki Yahata, do Departamento de Biologia do Desenvolvimento da Faculdade de Medicina da Universidade de Saúde de Fujita, no Japão, desenvolveu uma tecnologia capaz de modificar os níveis de heteroplasmia em células cultivadas portadoras da mutação m.3243A>G. O artigo foi disponibilizado online em 20 de março de 2025 e será publicado na edição de 10 de junho de 2025 (Volume 36, Edição 2) da revista Molecular Therapy Nucleic Acids. O trabalho teve coautoria do Dr. Yu-ichi Goto, do Centro Nacional de Neurologia e Psiquiatria, e do Dr. Ryuji Hata, da Organização Hospitalar da Prefeitura de Osaka.
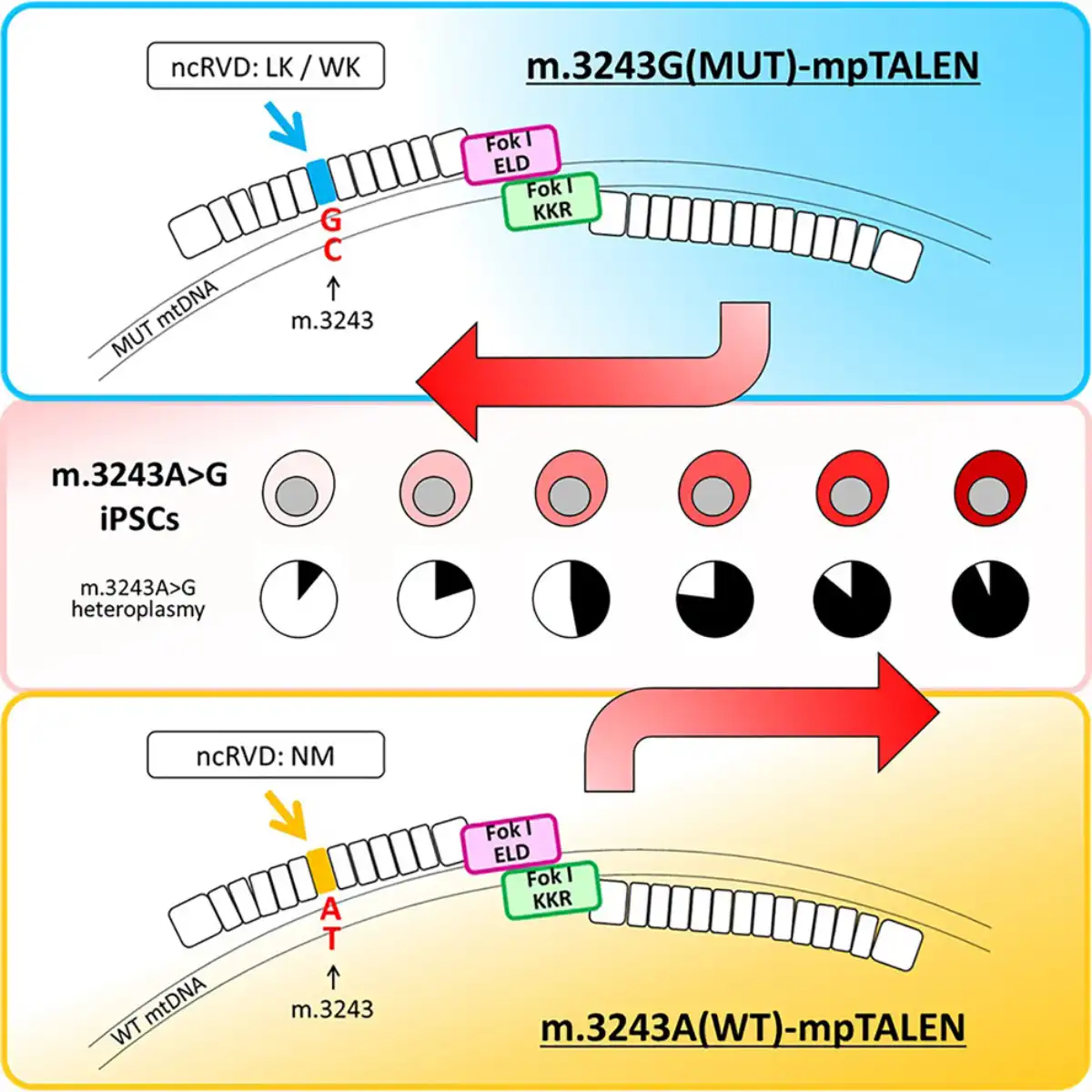
No artigo, os autores descrevem o desenvolvimento e uso de nucleases do tipo TALEN ativadoras de transcrição otimizadas e direcionadas ao mtDNA com platina (mpTALENs) — enzimas especializadas que podem atingir e clivar seletivamente sequências específicas de DNA. Os pesquisadores primeiro estabeleceram culturas de células-tronco pluripotentes induzidas (iPSCs) derivadas de pacientes contendo a mutação m.3243A>G e, em seguida, projetaram duas versões do sistema mpTALEN: uma para destruir o mtDNA mutante e outra para destruir o mtDNA normal. Essa abordagem bidirecional permitiu gerar células com cargas mutacionais variando de apenas 11% até 97%, mantendo, ao mesmo tempo, a capacidade de diferenciação dessas células em diversos tipos de tecidos. “Nosso estudo é o primeiro a demonstrar um aumento na proporção de mtDNA patogênico por meio de nucleases programáveis”, observa o Dr. Yahata.
As principais inovações da abordagem incluíram o uso de novos resíduos variáveis de dipeptídeos não convencionais e domínios de nucleases FokI heterodiméricos obrigatórios, o que aumentou a especificidade da tecnologia e reduziu a degradação indesejada de mtDNA fora do alvo. A equipe também utilizou técnicas adicionais, como a suplementação com uridina, para estabelecer linhagens celulares estáveis com diferentes cargas mutacionais, inclusive aquelas que normalmente teriam desvantagens de crescimento. “Nossos resultados demonstram que o processo de otimização das mpTALENs criou uma ferramenta útil para alterar os níveis de heteroplasmia em iPSCs com a mutação m.3243A>G, ampliando seu potencial para o estudo da patologia dessas mutações. Essa eficiência aprimorada também representa uma promessa para o uso das mpTALENs em estratégias terapêuticas para tratar pacientes com doenças mitocondriais relacionadas à mutação m.3243A>G”, afirma Yahata.
- Veja também: Transformando células da pele em neurônios.
De forma geral, o estudo representa um avanço significativo na medicina mitocondrial por várias razões. Primeiro, ele fornece aos pesquisadores diversas linhagens celulares isogênicas — geneticamente idênticas entre si — que diferem apenas no nível de heteroplasmia, permitindo o estudo preciso de como a carga mutacional afeta a manifestação da doença. Segundo, sugere que a tecnologia mpTALEN pode ter valor terapêutico no futuro, ao permitir a redução da carga de mtDNA mutante em pacientes.
“Nosso método proposto pode ser adaptado para outras mutações no mtDNA e contribuir para a compreensão de suas respectivas patologias, além de possibilitar o desenvolvimento de novos tratamentos, beneficiando potencialmente pacientes com diferentes formas de doenças mitocondriais”, conclui o Dr. Yahata.