Anne Trafton | MIT News
Преобразование одного типа клеток в другой — например, клетки кожи в нейрон — может быть осуществлено посредством процесса, который требует, чтобы клетка кожи была индуцирована в «плюрипотентную» стволовую клетку, а затем дифференцирована в нейрон. Исследователи из Массачусетского технологического института теперь разработали упрощенный процесс, который обходит стадию стволовой клетки, преобразуя клетку кожи непосредственно в нейрон.
Работая с клетками мышей, исследователи разработали метод преобразования, который является высокоэффективным и может производить более 10 нейронов из одной клетки кожи. Если воспроизвести этот подход в клетках человека, он может позволить генерировать большое количество двигательных нейронов, которые потенциально могут быть использованы для лечения пациентов с травмами спинного мозга или заболеваниями, нарушающими подвижность.
«Мы смогли получить результаты, на которых мы могли бы задать вопросы о том, могут ли эти клетки быть жизнеспособными кандидатами для клеточной заместительной терапии, на что мы надеемся. Вот куда нас могут привести эти типы технологий перепрограммирования», — говорит Кэти Гэллоуэй, профессор по развитию карьеры в области биомедицинской инженерии и химической инженерии WM Keck.
В качестве первого шага к разработке этих клеток в качестве терапевтического средства исследователи продемонстрировали, что они могут генерировать двигательные нейроны и трансплантировать их в мозг мышей, где они интегрируются с тканями хозяина.
Гэллоуэй является старшим автором двух статей, описывающих новый метод, которые сегодня опубликованы в Cell Systems . Аспирант Массачусетского технологического института Натан Ван является ведущим автором обеих статей.
От кожи к нейронам
Почти 20 лет назад ученые из Японии показали, что, доставляя четыре фактора транскрипции в клетки кожи, они могут заставить их стать индуцированными плюрипотентными стволовыми клетками (iPSC). Подобно эмбриональным стволовым клеткам, iPSC могут дифференцироваться во многие другие типы клеток. Этот метод хорошо работает, но он занимает несколько недель, и многие клетки не полностью переходят в зрелые типы клеток.
«Часто одной из проблем перепрограммирования является то, что клетки могут застрять в промежуточных состояниях», — говорит Гэллоуэй. «Поэтому мы используем прямую конверсию, когда вместо прохождения через промежуточное состояние iPSC мы переходим напрямую от соматической клетки к двигательному нейрону».
Исследовательская группа Гэллоуэй и другие уже демонстрировали этот тип прямой конверсии, но с очень низким выходом — менее 1 процента. В предыдущей работе Гэллоуэй использовала комбинацию из шести факторов транскрипции и двух других белков, стимулирующих пролиферацию клеток. Каждый из этих восьми генов доставлялся с использованием отдельного вирусного вектора, что затрудняло обеспечение того, чтобы каждый из них был экспрессирован на правильном уровне в каждой клетке.
В первой из новых статей журнала Cell Systems Гэллоуэй и ее студенты сообщили о способе оптимизации процесса, благодаря которому клетки кожи можно преобразовать в двигательные нейроны, используя всего три фактора транскрипции, а также два гена, которые переводят клетки в состояние высокой пролиферации.
Используя мышиные клетки, исследователи начали с исходных шести факторов транскрипции и экспериментировали с их исключением по одному, пока не достигли комбинации из трех — NGN2, ISL1 и LHX3 — которая могла успешно завершить преобразование в нейроны.
После того как число генов сократилось до трех, исследователи смогли использовать один модифицированный вирус для доставки всех трех из них, что позволило им гарантировать, что каждая клетка экспрессирует каждый ген на правильном уровне.
Используя отдельный вирус, исследователи также доставили гены, кодирующие p53DD и мутировавшую версию HRAS. Эти гены заставляют клетки кожи делиться много раз, прежде чем они начнут преобразовываться в нейроны, что позволяет получить гораздо более высокий выход нейронов, около 1100 процентов.
«Если бы вы экспрессировали факторы транскрипции на действительно высоком уровне в непролиферативных клетках, то скорость перепрограммирования была бы очень низкой, но гиперпролиферативные клетки более восприимчивы. Это как будто их потенцировали для конверсии, а затем они стали гораздо более восприимчивыми к уровням факторов транскрипции», — говорит Гэллоуэй.
Исследователи также разработали немного иную комбинацию факторов транскрипции, которая позволила им выполнить ту же прямую конверсию с использованием человеческих клеток, но с более низкой эффективностью — от 10 до 30 процентов, по оценкам исследователей. Этот процесс занимает около пяти недель, что немного быстрее, чем сначала преобразовать клетки в iPSC, а затем превратить их в нейроны.
Имплантация клеток
После того, как исследователи определили оптимальную комбинацию генов для доставки, они начали работать над лучшими способами их доставки, что и стало темой второй статьи журнала Cell Systems .
Они опробовали три разных вируса доставки и обнаружили, что ретровирус достиг наиболее эффективной скорости преобразования. Уменьшение плотности клеток, выращенных в чашке, также помогло улучшить общий выход двигательных нейронов. Этот оптимизированный процесс, который занимает около двух недель в мышиных клетках, достиг выхода более 1000 процентов.
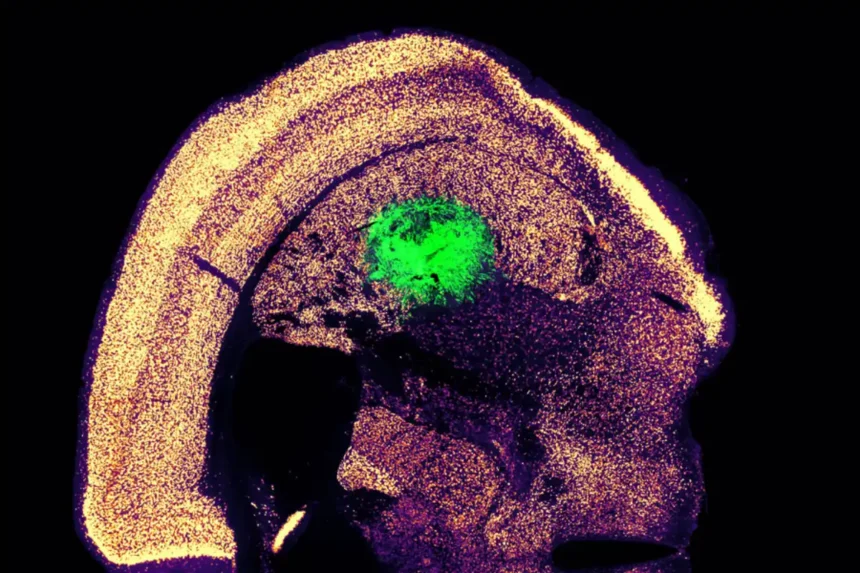
Работая с коллегами из Бостонского университета, исследователи затем проверили, можно ли успешно привить эти двигательные нейроны мышам. Они доставили клетки в часть мозга, известную как полосатое тело, которое участвует в контроле движений и других функциях.
Через две недели исследователи обнаружили, что многие нейроны выжили и, по-видимому, формируют связи с другими клетками мозга. При выращивании в чашке эти клетки показали измеримую электрическую активность и кальциевую сигнализацию, что предполагает способность общаться с другими нейронами. Теперь исследователи надеются изучить возможность имплантации этих нейронов в спинной мозг.
Команда MIT также надеется повысить эффективность этого процесса для преобразования человеческих клеток, что может позволить генерировать большие количества нейронов, которые могут быть использованы для лечения травм спинного мозга или заболеваний, влияющих на контроль движений, таких как БАС. Клинические испытания с использованием нейронов, полученных из iPSC, для лечения БАС в настоящее время ведутся, но увеличение количества клеток, доступных для такого лечения, может облегчить их тестирование и разработку для более широкого использования на людях, говорит Гэллоуэй.
Исследование финансировалось Национальным институтом общих медицинских наук и Программой стипендий для аспирантов Национального научного фонда.
Перепечатано с разрешения MIT News.